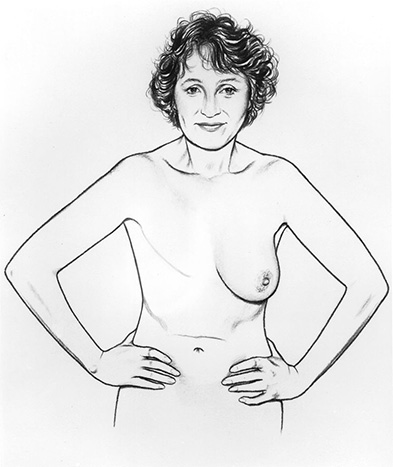
سرطان الثدي
سرطان الثدي هو أكثر أنواع السرطان شيوعًا بين النساء في فرنسا ويصيب امرأة واحدة من أصل 10. إذا اكتشفت مبكرًا ، فإن فرص الشفاء مهمة للغاية. في الواقع ، يمكن علاج سرطان الثدي في 9 من أصل 10 حالات إذا كان حجم الورم أقل من 1 سم ولا توجد غدد لمفاوية.
في عام 2012 ، تم اكتشاف 48000 حالة جديدة ، واليوم (2015) يقدر معدل البقاء على قيد الحياة الكلي بعد 5 سنوات من تشخيص سرطان الثدي بنحو 89 ٪ ، وجميع الأنواع مجتمعة.
الفحص
متوسط العمر للكشف عن سرطان الثدي هو 61 سنة. هذا هو السبب في أنه من المهم تحديد تشخيص السرطان المحتمل في أقرب وقت ممكن. يتم الفحص عادةً بواسطة طبيب نسائي ، ولكن يمكن القيام به أيضًا بواسطة طبيب عام أو قابلة. للنساء يتم تنظيم أكثر من 50 فحص مجاني. كل سنتين ، تتم دعوة النساء من سن 50 إلى 74 لزيارة مركز معتمد من اختيارهم لهذا الفحص المنظم.
سرطان الثدي
الخطوة الأولى في تشخيص سرطان الثدي هي الفحص السريري الذي يقوم به طبيب النساء. هذا ملامسة للثدي يمكن أن تحدد علامات ظهور الورم ، فمن المستحسن أن يبدأ هذا الفحص السريري من 25 عامًا. العلامات التي يجب مراقبتها أثناء هذا الاختبار هي:
ظهور كرة في الثدي: تقييم حجمها ، حركتها ، موقعها.
مظهر الجلد: ظهور احمرار ، تعديل الجلد.
شكل الحلمة والهالة: تشوه ، تراجع أو تقرح الحلمة و / أو الهالة. ظهور تدفق ملون من الدم من خلال الحلمة.
جس العقيدات: خاصة في الإبطين. الكشف عن العقد غير الطبيعية ، وزيادة حجم الغدد الليمفاوية بالقرب من الثديين.
التصوير الشعاعي للثدي
إنها الأشعة السينية للثدي التي توفر صوراً للثدي الداخلي باستخدام الأشعة السينية وتسلط الضوء على أنواع السرطان الصغيرة ، في مرحلة مبكرة قبل ظهور الأعراض. يحدث ذلك عندما يتم الكشف عن خلل في وقت الفحص السريري وكل سنتين للنساء أكثر من 50 ، كجزء من الفحص المنظم.
أثناء التصوير الشعاعي للثدي ، يقف المريض منتصبًا في خزانة الأشعة ويقف أمام جهاز الأشعة السينية الماموجرام. يتم ضغط الثدي بين لوحة ضغط بلاستيكية وحامل الفيلم. تؤخذ الأشعة السينية لكل الثدي ، واحدة في الجبهة وواحدة في منحرف. يستمر فحص تصوير الثدي بالأشعة حوالي 10 دقائق وهو غير مؤلم ، حتى لو لم يكن ذلك ممتعًا دائمًا للمريض.
في الماموجرام ، ينتج عن الورم كتلة بيضاء أو نقاط صغيرة تعكس التكلس الدقيق الذي يمكن أن تحدد خصائصه وجود أو عدم وجود السرطان.
يحدث ذلك عندما يتم الكشف عن خلل أثناء التصوير الشعاعي للثدي ، أو عندما يتم الكشف عن خلل أثناء الفحص السريري للنساء دون سن 30 سنة. بالنسبة للنساء دون سن 30 ، يوصى بإجراء تصوير بالموجات فوق الصوتية للثدي بدلاً من تصوير الثدي بالأشعة السينية بسبب كثافة الثدي التي لا تسمح بالحصول على صور واضحة.
يستخدم الموجات فوق الصوتية الموجات فوق الصوتية (موجات صوتية عالية التردد غير ضارة) للحصول على صور دقيقة من داخل الثدي والآفات المكتشفة أثناء التصوير الشعاعي للثدي.
الفحص غير مؤلم ويستغرق حوالي 20 دقيقة. يتم تطبيق هلام هيبوالرجينيك على صدر المريض لضمان اتصال مثالي بين الجلد وجهاز الموجات فوق الصوتية. ثم يطبق المجس بقوة على الثدي ويتم توجيهه في جميع الاتجاهات لمراقبة نسيج الثدي بأكمله وتحديد الغدد الليمفاوية غير الطبيعية. تظهر الحالات الشاذة باختلاف التناقضات بين الأخير والمناطق الصحية.
لا يمكن إجراء تشخيص للسرطان إلا بعد دراسة ، على المستوى المجهري ، طبيعة الخلايا التي تتكون منها الآفة التي حددتها تقنيات التصوير الموصوفة سابقًا ، وهذا هو الفحص المرضي لجزء من النسيج. الثدي. يختار الطبيب طريقة أخذ العينات وفقا لخصائص الآفة.
عوامل الخطر لسرطان الثدي
إن تحول الخلية السليمة إلى خلية سرطانية ينطوي على العديد من العوامل التي تؤثر على خطر هذا التحول. لا يستند تعريف عوامل الخطر لسرطان الثدي إلى اليقين المطلق. قد لا يصاب الشخص المصاب بعامل خطر واحد أو أكثر بالسرطان ، وعلى العكس من ذلك ، فإن الشخص الذي لا يوجد لديه عامل خطر قد يصاب بسرطان الثدي. وبالتالي ، فإن العلاقة بين عوامل الخطر المختلفة وتطور سرطان الثدي ليست واضحة دائمًا. هناك فئتان من عوامل الخطر ، عوامل الخطر الخارجية وعوامل الخطر الداخلية.
ترتبط عوامل الخطر الخارجية بالبيئة والظروف ونمط الحياة. هذه العوامل قد تفسر أكثر من 50 ٪ من سرطانات الثدي.
تعرض الجسم للهرمونات الاصطناعية: المواد الكيميائية التي تعد بدائل الاستروجين هي تلك التي تسبب سرطان الثدي بشكل شائع. وتسمى هذه المنتجات اضطرابات هرمونية أو الغدد الصماء. هرمون الاستروجين هو هرمون يشارك في تكاثر خلايا الثدي ، وبالتالي كلما زادت كمية هذا الهرمون في الجسم ، زاد خطر تطوير خلايا الورم في الثدي.
التعرض للإشعاع الطبي: قد يؤدي التشعيع المتكرر للصدر ، على سبيل المثال أثناء العلاج الإشعاعي لعلاج أنواع السرطان الأخرى ، إلى زيادة خطر حدوث سرطان الثدي. تتناسب درجة المخاطرة مع جرعة الإشعاع المستلمة وعمر المريض.
استهلاك التبغ والكحول: يزيد استهلاك التبغ والمشروبات الكحولية من تطور العديد من أنواع السرطان بما في ذلك سرطان الثدي. التدخين السلبي والنشط هو عامل خطر مهم في تطور سرطان الثدي.
يزيد استهلاك الكحول من مستويات الإستروجين التي تؤثر بشكل مباشر على حدوث سرطان الثدي. تكون الزيادة في المخاطر كبيرة عندما يكون الاستهلاك أكبر من مشروب واحد في اليوم ، و 10٪ لكل كوب من الكحول يستهلك أكثر في اليوم.
زيادة الوزن: خلال فترة انقطاع الطمث ، تعتبر زيادة الوزن (مؤشر كتلة الجسم بين 25 و 29.9) والسمنة (مؤشر كتلة الجسم أكبر من أو يساوي 30) من عوامل الخطر لحدوث سرطان الثدي. يمكن تفسير ذلك من خلال حقيقة أن الأنسجة الدهنية تخزن بسهولة الهرمونات المرتبطة بالسرطان. على العكس من ذلك ، فإن النشاط البدني المنتظم وكذلك اتباع نظام غذائي صحي ونوع البحر الأبيض المتوسط (غني بالخضروات والفواكه والحبوب ...) يمنع ظهور سرطان الثدي.
كما ذكرنا من قبل ، فإن عوامل الخطر هذه ليست دائمًا سبب الإصابة بسرطان الثدي ، ولكنها يمكن أن تعزز تطوره.
عوامل الخطر الداخلية ، والمعروفة أيضًا باسم عوامل الخطر المحددة ، هي مكونات للأفراد.
العمر: بشكل عام ، يزيد خطر الإصابة بسرطان الثدي مع تقدم العمر. 10 ٪ من سرطانات الثدي تحدث قبل سن 35 ، و 20 ٪ قبل سن 50. في عام 2012 ، كان متوسط عمر تشخيص سرطان الثدي 63 عامًا. يتم تشخيص نصف سرطانات الثدي بين سن 50 و 69 ، و 28 ٪ من سرطانات تحدث بعد سن 69. ساعدت هذه البيانات في تأسيس فحص منظم لسرطان الثدي للنساء من سن 50 إلى 74 عامًا. كل سنتين ، تتم دعوة النساء في هذه الفئة العمرية للذهاب إلى مركز فحص معتمد من اختيارهن لتلقي تصوير الثدي بالأشعة المغطاة بالكامل بواسطة الضمان الاجتماعي.
الإشباع الهرموني: هو معدل الاستروجين والبروجستيرون الذي تعرضت له المريض أثناء حياتها. ونتيجة لذلك ، يزداد خطر الإصابة بسرطان الثدي زيادة طفيفة لدى النساء اللائي تعرضن لأول مرة قبل سن 12 (تزداد المخاطر بنسبة 5٪ سنويًا قبل سن 12) وفي النساء اللائي وقع انقطاع الطمث لديهم بعد 55 عامًا (يزيد الخطر بنسبة 3٪ سنويًا بعد 55 عامًا) ، لأن مستوى هرمون الاستروجين لديهم أعلى ، وبالتالي فإن احتمال تطوير خلايا السرطان في الثدي أعلى. النساء اللواتي لم ينجبن أطفالًا أو الذين لم يرضعوا هم أكثر عرضة للإصابة بسرطان الثدي.
الاستعدادات الوراثية
تاريخ العائلة: يحدث ما بين 20 ٪ إلى 30 ٪ من سرطانات الثدي لدى النساء مع تشخيص حالة واحدة على الأقل من سرطان الثدي في الأسرة. يكون الخطر أكبر مرتين إذا تم اكتشاف سرطان الثدي الأول لدى قريب من الدرجة الأولى (الأم ، الأخت ، الابنة) قبل انقطاع الطمث. في هذه الحالة ، إذا كان السرطان قد أثر على كلا الثديين ، تتضاعف المخاطر. المخاطر أكبر أيضًا حسب عمر الوالد ، وكلما كان أصغر ، زادت المخاطر. الأشخاص الذين لديهم فرد من العائلة مصاب بسرطان المبيض أو سرطان القولون معرضون أيضًا لخطر الإصابة بسرطان الثدي. وأخيراً ، إذا كان رجل في الأسرة مصابًا بسرطان الثدي ، فالمخاطر أكبر.
الطفرات الوراثية التي تم تحديدها: إذا أصيب عدة أشخاص من نفس العائلة بسرطان الثدي خلال حياتهم ، فقد يكون هذا بسبب شذوذ وراثي ينتقل من جيل إلى آخر.
أظهرت الدراسات المختلفة تورط عدة جينات من المحتمل أن تصاب بسرطان الثدي ، بما في ذلك جينات BRCA 1 و BRCA2. BRCA تعني كلمة BReast Cancer ، وهي سرطان الثدي الإنجليزية. عندما تلاحظ طفرة في هذه الجينات ، هناك تكاثر غير طبيعي للخلايا وزيادة خطر الإصابة بسرطان الثدي. معدل سكان العالم الذين لديهم طفرة في هذه الجينات حوالي 1 ‰. النساء المصابات بهذه الحالة معرضات لخطر الإصابة بسرطان الثدي بنسبة تتراوح بين 65 ٪ و 85 ٪ قبل سن 70. تجدر الإشارة إلى أن جميع النساء المصابات بطفرة جين BRCA 1 و / أو BRCA 2 من غير المحتمل أن يصبن بسرطان الثدي. يوصى بإجراء اختبار جيني للطفرات للأشخاص الذين لديهم تاريخ عائلي من سرطان الثدي أو المبيض.
مع ذلك ، تجدر الإشارة إلى أن 5٪ إلى 6٪ فقط من سرطانات الثدي في عائلة طور فيها العديد من الأعضاء علم الأمراض ، ترتبط بتحول جيني لجينات BRCA 1 و BRCA 2.
لا تفسر عوامل الاختطار المختلفة هذه تطور سرطان الثدي ولكنها تزيد من خطر ظهور المرض ، لذلك يجب علينا مراقبته للحفاظ على صحته.
يتم تحديد مراحل سرطان الثدي من خلال الاختبارات التشخيصية. تعتمد مرحلة سرطان الثدي على ثلاثة معايير: حجم وتسلل الورم ، تورط أو عدم وجود الغدد الليمفاوية وأخيرا وجود أو عدم وجود نقائل. من هذه المعايير الثلاثة ، يتم تعريف مرحلة السرطان وفقًا لتصنيف TNM (الورم ، العقد ، ورم خبيث) المحدد من قِبل الاتحاد الدولي لمكافحة السرطان (UICC) واللجنة الأمريكية المشتركة للسرطان (AJCC).
حجم وتسلل الورم
يعتمد تسلل الورم على نزوح الخلايا السرطانية عبر طبقات غشاء مختلفة من الأنسجة. تتشكل الخلايا السرطانية في البداية على مستوى قنوات الحليب (منتجي الحليب) أو على مستوى الفصيصات ، نتحدث على التوالي عن سرطان الأقنية وسرطان الفص. إذا كانت خلايا الورم تعبر الأغشية القاعدية للفصيص أو القناة ، يصبح الورم غازيًا أو غازيًا.
يتوافق هذا المعيار الأول مع الحرف "T" من تصنيف TNM. لكل معيار ، ترتبط درجة تتراوح من 0 إلى 4:
تكساس: لا يمكن تقييم الورم
T0: الورم ليس واضحًا
T1: حجم الورم ≤ 2 سم في أكبر بعده و / أو الغزو الجزئي ≤ 1 ملم في أكبر بعده
T2: حجم الورم بين 2 سم و 5 سم في أكبر أبعادها
T3: حجم الورم ˃ 5 سم في أكبر بعده
T4: للورم امتداد مباشر لجدار الصدر أو الجلد ، بغض النظر عن حجمه.
وفقًا لهذه المعايير الثلاثة ودرجتها ، تم تحديد خمس مراحل للنهوض بسرطان الثدي. ويلاحظ هذه المراحل في الأرقام الرومانية:
0: الخلايا السرطانية موجودة في غشاء القناة الأقنية ، أو سرطان الأقنية في الموقع ، أو في غشاء سرطان مفصص ، مفصص في الموقع.
I: حجم الورم السرطاني هو 2 سم أو أقل ، ولم ينتشر السرطان خارج الثدي ، سواء إلى الغدد الليمفاوية أو إلى أماكن بعيدة أخرى.
الثاني: حجم الورم ما بين 2 و 5 سم ، و / أو السرطان قد انتشر إلى الغدد الليمفاوية المجاورة (الإبطية ، الثديية ، تحت الترقوة ، الغدد الليمفاوية فوق الترقوية).
ثالثًا: انتشر السرطان إلى العقد اللمفاوية المجاورة وربما إلى الأنسجة المجاورة أيضًا.
رابعا: انتشر السرطان إلى أجزاء أخرى من الجسم بالإضافة إلى العقد اللمفاوية القريبة من الثدي ، مثل العظام والكبد والرئتين والدماغ والغدد الليمفاوية البعيدة من الثدي.
درجة سرطان الثدي تجعل من الممكن تحديد عدوانية ، وسرعته في الانتشار ، وبالتالي تحديد العلاجات المناسبة. يتم تعريفه بعد الفحص التشريحي لعينة خلية تم الحصول عليها خلال الخزعة. يقوم الطبيب الفاحص بتقييم ثلاث معلمات مورفولوجية ، ويحدد لكل معلمة درجة من 1 إلى 3. وكلما ارتفعت درجة ، زاد تطور سرطان الثدي.
العمارة السرطانية: هذا هو ظهور الخلايا السرطانية. فكلما كانت الخلايا السرطانية تبدو مختلفة عن الخلايا الطبيعية ، كلما كانت أكثر عدوانية لأنها غير متمايزة. فقدت الخلايا غير المتمايزة وظيفتها الأصلية ، لم يعد لديها أي بنية مماثلة للخلايا الطبيعية. بالنسبة لهذا المعيار ، تتطابق الملاحظة 1 مع حقيقة أن الورم يحتوي على العديد من الهياكل المتشكلة جيدًا ، ويشبه الخلايا غير الورمية. في حين أن الملاحظة 3 تتوافق مع الخلايا السرطانية التي تحتوي على هياكل ضئيلة أو معدومة جيدًا.
ظهور النواة: تحتوي الخلايا السرطانية على نواة مختلفة عن الخلايا الطبيعية ، إما بحجمها أو شكلها. أدنى ملاحظة لهذه المعلمة هي النوى التي هي صغيرة الحجم ومنتظمة الشكل. الملاحظة 3 ، تتوافق مع النوى ذات الحجم الكبير ، والتي يختلف شكلها كثيرًا.
نشاط الانقسام الخيطي: كلما انقسمت الخلايا السرطانية كلما زاد خطر انتشار السرطان في الجسم وأصبح علاج السرطان أكثر صعوبة. يتم تحديد النشاط الانقسامي من خلال عدد الخلايا الانقسام ، أي التي تنقسم. بالنسبة لهذا المعيار ، تقابل النتيجة 1 عددًا صغيرًا من الانقسامات ، وبالتالي التقسيم البطيء للخلايا السرطانية. في حين أن الملاحظة 3 تتوافق مع التقسيم السريع للخلايا السرطانية وعدد كبير من الإنقباضات.
لتحديد درجة سرطان الثدي ، أضف درجات مختلفة تم الحصول عليها عند توصيف المعلمات الموضحة أعلاه. المبلغ الذي تم الحصول عليه يتوافق مع الدرجة من الأول إلى الثالث ، والتي تسمى الدرجة النسيجية من إيلستون إليس.
هناك علاجات مختلفة لسرطان الثدي تحددها المرحلة ونوع السرطان. هذه العلاجات لها أهداف مختلفة:
إزالة الورم أو الانبثاث
تقليل خطر إعادة المخالف
إبطاء تطور الورم أو النقائل
علاج الأعراض الناجمة عن المرض
في بعض الأحيان ، هناك نوع واحد فقط من العلاج يكفي لعلاج سرطان الثدي. في حالات أخرى ، هناك حاجة إلى مزيج من العلاجات. كل مريض مختلف وكل سرطان فريد من نوعه ، ويتم اختيار العلاج المناسب من خلال استشارة متعددة التخصصات من قبل العديد من الأطباء.
علاجات سرطان الثدي - استئصال الثدي: هذا هو العلاج الأكثر استخدامًا في المقام الأول ، وهو يهدف إلى إزالة الأنسجة المصابة بالخلايا السرطانية. يتم إجراء نوعين من العمليات الجراحية: جراحة الثدي المحافظة تسمى استئصال الورم أو استئصال القطاع ، وجراحة الثدي غير المحافظة المسماة استئصال الثدي.
تتضمن الجراحة المحافظة إزالة الورم وجزء صغير من الأنسجة المحيطة من الورم للاحتفاظ بمعظم ثدي المريض. تُفضل هذه الجراحة في أسرع وقت ممكن ، ويكملها العلاج الإشعاعي لتجنب خطر التكرار. استئصال الورم ممكن بالنسبة للأورام الفردية الصغيرة ، وهذا يعني بتركيز واحد ، أو للأورام الصغيرة التي لها بؤرتان قريبتان.
تتضمن الجراحة غير المحافظة إزالة الثدي بالكامل ، بما في ذلك الهالة والحلمة. في هذه الحالة ، إذا سمحت حالة المريض ، يتم تقديم تقنيات إعادة بناء الثدي للمريض. يمكن أيضًا إزالة Ganglia جراحياً إذا كانت الإزالة ضرورية. يتم إجراء عملية استئصال الثدي إذا كان السرطان يؤثر على عدة مناطق وإذا كان حجم الورم مهمًا.
قد يخضع المريض لجراحات أخرى ، خاصة لتحديد انتشار الورم إلى العقد. يتم إجراء خزعة العقدة الليمفاوية الخافرة لتحديد ما إذا كانت الغدد الليمفاوية تتأثر أم لا. العقدة الليمفاوية المخففة هي العقدة الأولى التي تستقبل الليمفاوية من منطقة الثدي المحيطة بالورم. إذا تم الوصول إلى العقدة الليمفاوية الخافرة ، فهذا يعني أن هناك خطورة كبيرة في أن تكون الغدد الليمفاوية الإبطية ، وفي هذه الحالة ننتقل إلى فترة توقف للعقد الإبطية.
راحة الغدد الليمفاوية الإبطية ، والتي هي الغدد الليمفاوية للإبط ، تسمح بإزالتها. تتم هذه الجراحة في نفس الوقت الذي يتم فيه استئصال الثدي.
يستخدم العلاج الإشعاعي إشعاعات مؤينة عالية الطاقة لتدمير الخلايا السرطانية. هذه الطريقة تحافظ على الأنسجة والأعضاء المجاورة الصحية. لسرطان الثدي ، يمكن علاج أربعة مجالات في حالات مختلفة:
الغدة الثديية بعد الجراحة المحافظة ؛
سرير الورم بعد الجراحة المحافظة.
جدار الصدر بعد الجراحة غير المحافظة ؛
العقد من سلسلة الثدي الداخلية والغدد الليمفاوية فوق الترقوة.
كل علاج إشعاعي فريد من نوعه وتعتمد الجرعة المعطاة على المريض وسرطان الثدي. يتم إعطاء العلاج الإشعاعي دائمًا بعد جراحة الثدي المحافظة وأحيانًا بعد استئصال الثدي. أنه يقلل من خطر تكرار سرطان الثدي. العلاج الإشعاعي روتيني للسرطانات التي انتشرت إلى مناطق كبيرة من العظام وشكلت نقائل العظام.
العلاج الكيميائي هو علاج يعتمد على الأدوية التي تؤثر على انقسام الخلايا ، إنه علاج طبي. إنه علاج عام يؤثر على الجسم بأكمله ، جميع الخلايا السرطانية تتأثر بهذا العلاج ، سواء تم تشخيص وجودها أم لا. الأدوية المستخدمة هي أدوية مضادة للسرطان ، وتسمى أيضًا الأدوية السامة للخلايا. لا يتم تقديم هذا العلاج بشكل روتيني للمرضى. يوصى بالعلاج الكيميائي عندما تكون المرحلة وعامل الخطر للتكرار مرتفعين ، بالنسبة لسرطان الثدي المتقدم محليًا ، أي الورم كبير الحجم ولا يمكن إزالته عن طريق الجراحة ، وكذلك فقط للسرطانات التي انتشرت إلى الغدد الليمفاوية ومناطق أخرى من الثدي ، ولكن ليس إلى أجزاء أخرى من الجسم. يتم علاج سرطانات الثدي المبكرة ذات الخطورة العالية للتكرار أيضًا بالعلاج الكيميائي ، وكذلك السرطانات المنتشرة.
في معظم الأحيان ، يوصف العديد من الأدوية المضادة للسرطان في تركيبة ، والتي تسمح لتدمير الخلايا السرطانية عن طريق وقف انقسام الخلايا. يتم إعطاء هذه الأدوية عن طريق الوريد بشكل عام في المستشفى ، مع بعض الاستثناءات التي تكون في شكل أقراص تؤخذ عن طريق الفم.
العلاج الكيميائي ينتج العديد من الآثار الجانبية المختلفة. يعتمد تواتر ونوع التأثير الجانبي على الشخص ونوع المادة السامة للخلايا المستخدمة والجرعة. لا يتعرض المرضى لهذه الأحداث السلبية بشكل روتيني ، ولكن إذا كان الأمر كذلك ، فهناك علاجات لتخفيف المرضى.
العلاج بالهرمونات هو علاج نظامي ، أي الجسم كله ، يبطئ نمو وانتشار الخلايا السرطانية عن طريق تغيير مستويات الهرمونات في الثدي. بعض أورام الثدي حساسة للهرمونات ، مما يعني أن نموها يتم تحفيزه عن طريق الهرمونات الأنثوية والبروجستيرون والإستروجين. لذلك يهدف العلاج بالهرمونات إلى تقليل معدل هذه الهرمونات لتقليل تحفيزها. غالبًا ما يستخدم هذا العلاج في حالات السرطانات المبكرة منخفضة خطر التكرار ، وبالطبع فهي حساسة للهرمونات.
هناك نوعان من العلاج الهرموني:
العلاجات الدوائية التي تؤثر على الخلايا الحساسة للبروجسترون والإستروجين. في علاجات المخدرات ، نجد:
مضادات الإستروجين التي ترتبط بمستقبلات الإستروجين وبالتالي تمنع تحفيز الخلايا السرطانية بواسطة هذا الهرمون. أكثر مضادات الاستروجين المستخدمة هي عقار تاموكسيفين ، الذي يستخدم في كل من النساء بعد انقطاع الطمث وقبل انقطاع الطمث. في النساء بعد انقطاع الطمث ، يمكن إعطاء المخدر ، الذي يقلل من عدد المستقبلات على خلايا سرطان الثدي ، عن طريق العضل.
مضادات الروائح التي تمنع تصنيع هرمون الاستروجين عند النساء بعد انقطاع الطمث. Aromatase هو إنزيم تشارك في إنتاج هرمون الاستروجين. عن طريق تثبيط الروائح ، يتم تقليل مستوى الهرمونات في جميع أنحاء الجسم.
نظائرها هرمون الإفراج عن الهرمون (LH-RH) ، والتي تحفز إنتاج هذا الهرمون. LH-RH ، بواسطة الشلالات ، لها دور في إنتاج هرمون الاستروجين. نظائر LH-RH تسبب فرط تنشيط الغدة النخامية. بمجرد التحفيز المفرط ، لم تعد الغدة النخامية تحفز المبايض التي لم تعد تنتج هرمون الاستروجين. هذا العلاج يعادل التسبب في انقطاع الطمث لدى المريض. وهكذا يشرع هذا العلاج فقط للنساء الذين ليسوا بعد انقطاع الطمث.
العلاجات غير الدوائية التي تتكون من وقف إنتاج هرمون الاستروجين من المبايض عن طريق إزالتها عن طريق الجراحة (استئصال المبيض) أو إشعاعها (العلاج الإشعاعي). يتم إجراء الجراحة في النساء قبل انقطاع الطمث اللائي لم يعدن يرغبن في إنجاب أطفال.
يمكن اعتبار علاجات أخرى لسرطان الثدي: العلاجات البيولوجية و bisphosphonates. العلاجات البيولوجية تسد آليات الخلايا السرطانية ، وبالتالي تغيير سلوكها. يتم استخدامها في حالات سرطان الثدي المتقدمة ، النقيلي و / أو المعرضين لخطر كبير من تكرار ، أو لعلاج الآثار الجانبية للعلاج الكيميائي.
البايفوسفونيت يساعد في تقوية العظام ومنع انهيارها. لذلك يستخدم هذا العلاج لسرطانات الثدي التي لها نقائل العظام.